你会填吗
(1)地壳中元素含量:铁____铝。
(2)核外电子数:氯离子____氯原子。
(3)含碳量:甲醛 (CH2O)____醋酸 (C2H4O2)。
(4)金属与稀盐酸反应的剧烈程度:镁____铁。
(5)铜丝在火焰上灼烧,灼烧后的“铜丝”质量____原铜丝的质量。
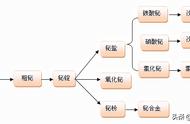
(6)武德合金(组成金属是铋、铅、锡、镉)可用来制电路保险丝、自动灭火装置等,其熔点____锡的熔点。
(7)若用氯酸钾和二氧化锰(催化剂)混合制取氧气,则二氧化锰在反应前后固体混合物中的质量分数:反应前________反应后。
不
要
偷
看
(1) 地壳中含量多的元素前五名是:氧、硅、铝、铁、钙,所以地壳中元素含量:铁小于铝。
(2) 氯离子是氯原子得电子得到的,所以核外电子总数:氯原子小于氯离子。
(3) 每个醋酸分子中含有的碳、氢、氧原子个数是每个甲醛分子中含有的碳、氢、氧原子个数的 2 倍,碳元素的质量分数相等。
(4) 由于镁的金属活动性比铁的金属活动性强,所以镁与稀盐酸反应的速率比铁与盐酸反应的速率快。
(5) 铜丝加热是铜吸收空气中的氧气后生成氧化铜,所以铜丝在火焰上灼烧,灼烧后的“铜丝”质量大于原铜丝的质量。
(6) 合金的熔点比各成分的熔点低,但硬度比各成分硬度高。
(7) 用氯酸钾和二氧化锰来制取氧气的反应原理:氯酸钾 催化剂催化剂__Δ 氯化钾 氧气,随着反应的进行生成氧气,使混合物的质量不断减小,而二氧化锰作催化剂,反应前后质量不变;故二氧化锰的质量分数会不断增大 。
【总结】水的作用
生命必需的水在化学中常用作溶剂和原料。
(1)
部分地下水含较多_________物质称为硬水;
酸雨中因含有导致土壤酸化_________;
海水中质量分数最高的元素是_________;
保持水的化学性质的最小微粒是_________。
(2)下列实验均用到水,其中仅作为溶剂的是()
A.配制 0.9% 的生理盐水
B.生石灰变成熟石灰
(3)下列两组固体物质用水即可鉴别的是_________
A.CuSO4,Na2SO4
B.NaCl,Na2SO4
(4)光催化分解水的过程是将光能转化为能。电解水制氢时,在与直流电源_________极相连的电极上产生 H2,该方法获得氢能的缺点是__________________。
不
要
偷
看
解析
(1) 部分地下水含较多的可溶性钙、镁化合物,这种水属于硬水;二氧化硫、氮氧化物等物质溶解在雨水中,能和水反应生成亚硫酸、硫酸、硝酸等物质,这些物质进入土壤中,能使土壤酸化,硫酸的化学式是 H2SO4;海水的主要成分是水,水中氧元素的质量分数大于氢元素的质量分数,所以海水中质量分数最高的元素是氧元素;水分子是保持水的化学性质的最小微粒,水的化学式是 H2O。
(2) 配制 0.9% 的生理盐水时,水作为溶剂,起到溶解氯化钠的作用;生石灰变成熟石灰时,生石灰和水反应生成熟石灰,水是反应物。
(3) 硫酸铜溶于水时,溶液是蓝色的,硫酸钠溶于水时,溶液是无色的,硫酸钠和硫酸铜用水就可以鉴别;而氯化钠和硫酸钠溶于水时,溶液都是无色的;
故选 A
(4) 光催化分解水的过程是将光能转化为化学能,电解水时,正极上产生的是氧气,负极上产生的是氢气,过程中消耗大量的电能。
答案
(1) 可溶性钙、镁化合物;H2SO4;氧元素;H2O
(2) A
(3) A
(4) 化学;负;消耗大量电能
欢迎关注*中学高分宝典